Fecundación in vitro paso a paso: qué ocurre en cada fase

Si estás leyendo sobre fecundación in vitro, probablemente no lo haces por curiosidad. Lo haces porque te lo han propuesto, porque lo estás valorando o porque ya estás dentro del proceso y quieres entender mejor qué va a ocurrir.
La FIV es un proceso médico organizado en fases, con decisiones en cada etapa y tiempos que conviene conocer. Comprender cómo se desarrolla, cuánto puede durar y qué factores influyen realmente en el resultado permite afrontar el tratamiento con mayor claridad y expectativas más ajustadas.
Cuando se habla de fecundación in vitro, muchas veces se piensa solo en el momento en que el óvulo y el espermatozoide se encuentran en el laboratorio. Sin embargo, ese es solo uno de los pasos de un recorrido más amplio.
En este artículo vamos a explicarlo de forma estructurada, para que puedas situarte en cada fase y entender qué ocurre en cada momento.
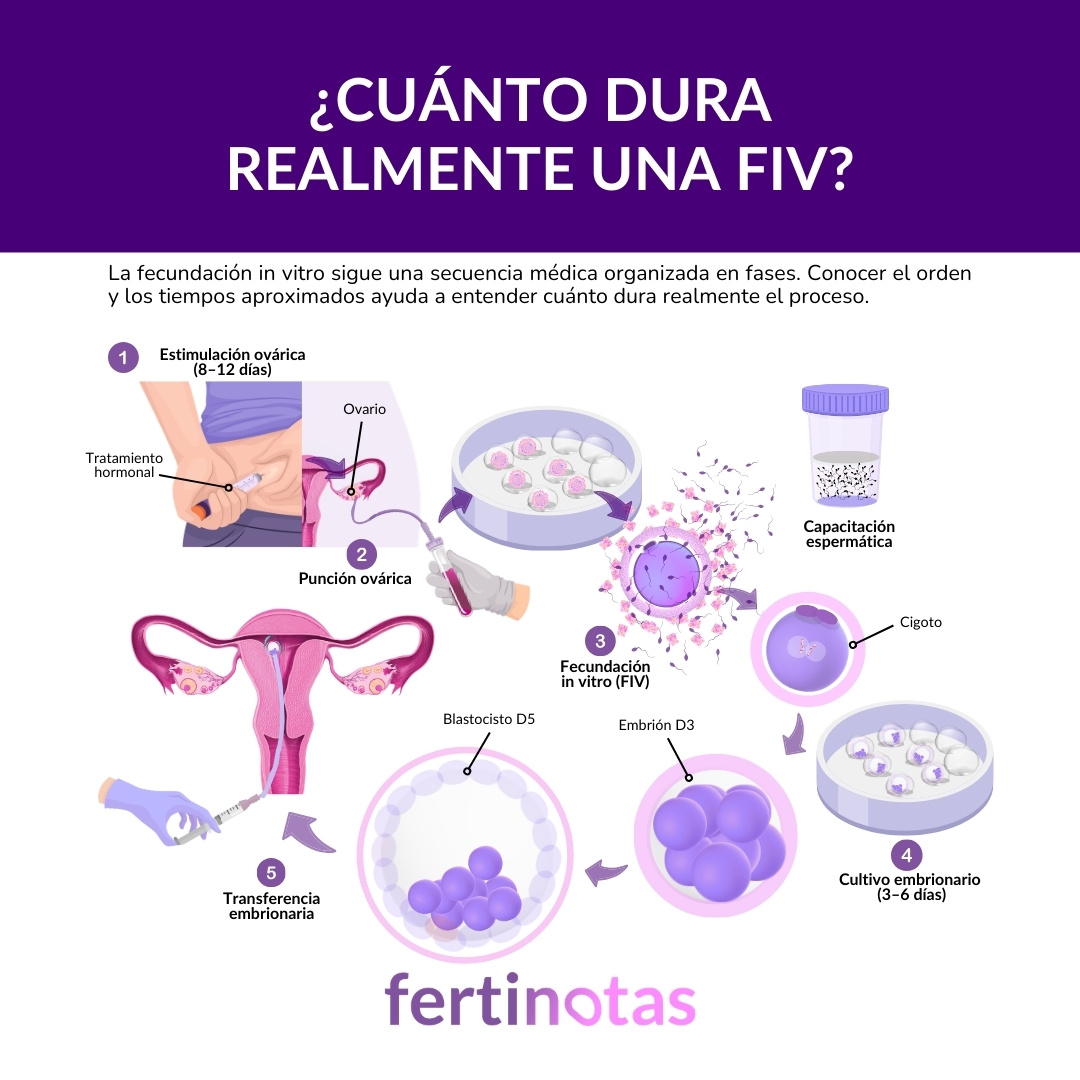
¿Cuánto dura realmente una FIV?
La duración de una fecundación in vitro no es exactamente igual para todas las personas, pero sí sigue un protocolo claro.
No es algo que se haga “sobre la marcha”. Se planifica en función del diagnóstico, la edad, la reserva ovárica, la calidad del semen y la técnica que esté indicada en cada caso.
Antes incluso de empezar la estimulación puede haber una fase preparatoria. A veces se bloquea el ciclo hormonal previo para organizar mejor la respuesta del ovario; en otras ocasiones se trabaja directamente sobre el ciclo natural.
Esta parte puede añadir algunas semanas al proceso, dependiendo de la estrategia elegida.
Cuando el tratamiento comienza, el calendario suele organizarse de esta manera:
• Estimulación ovárica: unos 8 a 12 días de medicación y controles.
• Punción ovárica: un procedimiento puntual para obtener los óvulos.
• Cultivo embrionario: normalmente entre 3 y 5 días, aunque algunos embriones alcanzan el estadio de blastocisto en día 6.
• Transferencia embrionaria: en el mismo ciclo o en uno posterior si se decide congelar.
Si además se realiza un estudio genético del embrión, este debe biopsiarse y vitrificarse, lo que implica que la transferencia se haga en un ciclo distinto.
Existen también variantes del tratamiento —óvulos propios o donados, semen fresco, congelado o procedente de biopsia testicular— que introducen matices técnicos, pero la secuencia médica sigue siendo la misma.
En términos generales, desde que empieza la estimulación hasta la prueba de embarazo suelen pasar entre cuatro y seis semanas. Si hay preparación previa o transferencia diferida, el proceso completo puede alargarse más.
Lo importante es entender que, aunque cada caso tiene particularidades, la FIV no es un proceso caótico. Tiene fases bien definidas y tiempos orientativos que el equipo adapta a cada situación.
La fase previa: diagnóstico y planificación personalizada
La FIV no empieza el día que se administran las hormonas. Empieza antes, con un diagnóstico preciso. Cada pareja llega a este punto por una situación concreta, y esa situación determina el tratamiento indicado.
Antes de iniciar una fecundación in vitro, el equipo médico necesita disponer de información actualizada sobre la realidad reproductiva de ese momento. Se valora la capacidad del ovario para responder a la estimulación —la reserva ovárica— teniendo en cuenta la edad y los antecedentes médicos.
Se analiza también la disponibilidad y calidad de los espermatozoides, porque el resultado depende de ambos gametos.
Se estudia el útero y el endometrio, es decir, el entorno donde deberá implantarse el embrión. No se trata solo de generar embriones, sino de asegurarse de que las condiciones para la implantación son adecuadas.
En casos en los que ha habido intentos previos sin éxito, la evaluación puede ampliarse. Existen pruebas que analizan la receptividad endometrial y permiten ajustar el momento exacto de la transferencia al periodo más favorable.
Entre ellas se encuentran estudios como el ERA (Endometrial Receptivity Analysis), así como otras pruebas complementarias que evalúan el entorno endometrial, como EMMA o ALICE. No forman parte del protocolo estándar en todos los casos, pero pueden considerarse cuando la historia clínica lo justifica.
A todo ello se suma la valoración de la salud general. Un embarazo exige al organismo un esfuerzo importante, y es necesario confirmar que no existen condiciones médicas que deban optimizarse antes de iniciar el tratamiento.
También se tiene en cuenta el momento vital. La FIV es un procedimiento médico, pero se desarrolla en un contexto personal. Afrontarlo con estabilidad y preparación no cambia la biología, pero sí influye en cómo se vive el proceso.
En esta fase se define la estrategia. No hay dos tratamientos idénticos, porque no hay dos diagnósticos iguales.

Estimulación ovárica: qué ocurre realmente en esta fase
En un ciclo natural, el ovario responde a señales hormonales que el propio cuerpo produce —principalmente FSH y, en menor medida, LH— y como resultado suele madurar un único folículo que liberará un óvulo.
En la fecundación in vitro se utiliza ese mismo mecanismo fisiológico, pero de forma controlada y con una intensidad mayor. Se administran fármacos que contienen, sobre todo, FSH —y en algunos casos combinaciones con LH— para estimular el crecimiento simultáneo de varios folículos. En determinados perfiles, especialmente en protocolos más suaves, pueden emplearse también moduladores como el citrato de clomifeno o letrozol, según la estrategia elegida.
Los medicamentos utilizados pueden ser gonadotropinas de origen urinario altamente purificadas o preparados recombinantes obtenidos por biotecnología. Ambos tipos son eficaces y seguros cuando se emplean correctamente; la elección depende del perfil clínico y del criterio médico.
La administración suele ser subcutánea, mediante pequeñas inyecciones diarias que la propia paciente puede aplicarse en casa, generalmente en la zona abdominal. Las agujas son finas y, aunque al principio pueden generar cierta aprensión, la mayoría de las mujeres las describen como manejables y poco dolorosas tras los primeros días.
Antes de iniciar esta fase ya se ha valorado la capacidad de respuesta del ovario. La edad, la reserva ovárica y los antecedentes permiten estimar qué dosis puede ser eficaz sin aumentar innecesariamente el riesgo de complicaciones. No se utilizan pautas estándar para todas las personas.
Durante aproximadamente 8 a 12 días se realizan controles ecográficos periódicos para medir el crecimiento de los folículos y, en muchos casos, determinaciones hormonales para comprobar que la respuesta es adecuada. Si es necesario, se ajusta la dosis.
Cuando los folículos alcanzan el tamaño esperado, se administra una última medicación —conocida como “disparo” de ovulación— que desencadena la maduración final de los ovocitos y permite programar la punción con precisión.
El objetivo es obtener un número suficiente de ovocitos que aumente las probabilidades acumuladas de éxito. Sin embargo, más no siempre significa mejor. La calidad ovocitaria, muy influida por la edad, es un factor determinante, y una respuesta equilibrada suele ser preferible a una respuesta excesiva.
La estimulación es, por tanto, un proceso dinámico y supervisado. Su seguimiento estrecho permite minimizar riesgos como el síndrome de hiperestimulación ovárica y adaptar el tratamiento en tiempo real.
Es habitual notar hinchazón abdominal leve o sensación de presión pélvica a medida que los folículos crecen. En la mayoría de los casos, estos síntomas son transitorios y desaparecen tras la punción.
Fecundación en el laboratorio: qué ocurre realmente ese día
En un embarazo natural, la fecundación ocurre en la trompa de Falopio. Millones de espermatozoides inician el recorrido, pero solo uno consigue atravesar las capas que rodean al óvulo e introducir su carga genética en su interior. Es un proceso de selección biológica y competencia celular.
En la fecundación in vitro, el laboratorio no “crea” la fecundación: facilita que ese encuentro ocurra en un entorno controlado.
El día de la punción, los ovocitos recuperados se identifican en el laboratorio y se evalúa su grado de madurez. Para que puedan ser fecundados deben encontrarse en una fase concreta del ciclo celular —la metafase II— que permite la entrada correcta del material genético masculino.
En paralelo, se prepara la muestra seminal. Se seleccionan los espermatozoides móviles y con mejor comportamiento funcional, eliminando restos celulares y plasma seminal. Si la muestra procede de congelación o de biopsia testicular, el procesamiento se adapta a esa circunstancia.
A partir de ahí, existen dos formas principales de facilitar la fecundación.
En la FIV convencional, los ovocitos se colocan en una pequeña gota de medio de cultivo junto con miles de espermatozoides.
En ese entorno controlado, son los propios espermatozoides los que compiten y uno de ellos penetra el ovocito. Es un proceso mediado por la capacidad natural del espermatozoide, pero en condiciones optimizadas.
En la ICSI (inyección intracitoplasmática de espermatozoides), el proceso es diferente. El ovocito se “denuda”, es decir, se retiran las células que lo rodean para poder evaluar su madurez y manipularlo.
Bajo un microscopio de alta precisión, el embriólogo selecciona un espermatozoide y lo introduce directamente en el interior del ovocito mediante una micropipeta extremadamente fina. Es una técnica de micromanipulación que requiere experiencia y pericia técnica, y que se utiliza cuando el factor masculino lo aconseja o cuando existen antecedentes de fallos previos de fecundación.
En ambos casos, el laboratorio no garantiza el desarrollo embrionario; facilita que la carga genética masculina y femenina puedan unirse en condiciones óptimas.
Al día siguiente se evalúa si la fecundación ha sido correcta. El signo clásico es la presencia de dos pronúcleos en el interior del ovocito, uno de origen materno y otro paterno, lo que indica que el material genético de ambos ha comenzado a organizarse para formar un nuevo embrión.
No todos los ovocitos maduros fecundan. De forma orientativa, la tasa de fecundación suele situarse en torno al 60–80% de los ovocitos maduros, aunque puede variar según la edad, la calidad ovocitaria y el factor masculino.
Este momento —la llamada del día siguiente— suele ser el primero en el que se obtiene una información concreta sobre cómo está evolucionando el ciclo.
En algunos casos, especialmente cuando existe fragmentación del ADN espermático, alteraciones importantes en la morfología o antecedentes de fallos repetidos de fecundación o implantación, pueden utilizarse técnicas adicionales de selección espermática.
Entre ellas se encuentran métodos como la IMSI (selección espermática con aumento microscópico superior), dispositivos microfluídicos que intentan imitar la selección natural del espermatozoide más competente, o sistemas basados en la capacidad del espermatozoide para unirse a ácido hialurónico (PICSI).
El objetivo de estas técnicas no es “mejorar” el espermatozoide, sino seleccionar aquellos con mejores características funcionales dentro de la muestra disponible. La evidencia científica muestra beneficios en determinados contextos, aunque no se utilizan de manera rutinaria en todos los casos.
Es importante entender que estas estrategias optimizan la selección, pero no modifican la carga genética del espermatozoide. Si existe una alteración genética, la técnica no la corrige; simplemente facilita elegir el gameto más competente dentro de lo disponible.
Desarrollo embrionario: valoración y posibles decisiones adicionales
Cuando el embrión alcanza el estadio de blastocisto —habitualmente en día 5 o 6— el embriólogo puede valorar con más detalle su estructura. En este momento ya se distinguen dos componentes fundamentales:
La masa celular interna, que dará lugar al futuro feto.
El trofoectodermo, que formará parte de la placenta.
La clasificación más utilizada evalúa tres aspectos:
• El grado de expansión del blastocisto, es decir, cuánto ha crecido y expandido su cavidad interna.
• La calidad de la masa celular interna.
• La calidad del trofoectodermo.
Por eso a veces se escuchan códigos como “4AA”, “3BB” o “5AB”. El número indica el grado de expansión; la primera letra corresponde a la masa celular interna y la segunda al trofoectodermo. Las categorías A describen una morfología más organizada, B una calidad intermedia y C una morfología menos favorable.
Esta clasificación es morfológica: se basa en lo que se observa al microscopio. No evalúa directamente la carga genética del embrión. En general, una mejor morfología se asocia a mayores probabilidades de implantación, pero no existe garantía absoluta.
Embriones con clasificación intermedia pueden dar lugar a embarazos evolutivos, y embriones de excelente aspecto pueden no implantar. La biología no es completamente predecible.
En este estadio también puede plantearse la biopsia embrionaria para realizar un estudio genético preimplantacional (PGT-A u otras indicaciones). Lo habitual es que esta posibilidad se haya discutido antes de iniciar el ciclo, especialmente si existen antecedentes de edad materna avanzada, abortos de repetición o alteraciones genéticas conocidas.
Sin embargo, en algunos casos, la evolución del ciclo puede llevar al equipo a revisar esa decisión y comentar nuevamente la opción con la pareja. Esta comunicación entre el equipo médico y el laboratorio es continua y forma parte del proceso.
Cuando se realiza biopsia, se extraen algunas células del trofoectodermo y el embrión se vitrifica a la espera del resultado genético. Este paso modifica el calendario del tratamiento, ya que la transferencia se realizará en un ciclo posterior.
Entender estos criterios ayuda a interpretar la información que se recibe del laboratorio y a situarla en su contexto clínico.
Entender el proceso para vivirlo con más calma
Tras la punción ovárica comienza una nueva fase del tratamiento. Aunque los ovarios han producido folículos y ovocitos, el entorno hormonal natural del ciclo se ha modificado por la estimulación.
Por eso, en la mayoría de los protocolos, se inicia suplementación con progesterona —y en algunos casos también con estrógenos— para asegurar que el endometrio se mantenga en condiciones adecuadas para la implantación.
La progesterona es fundamental para sincronizar el endometrio con el desarrollo embrionario. Puede administrarse por vía vaginal, subcutánea u oral, según el protocolo. Esta medicación se mantiene hasta el día de la prueba de embarazo.
Si el resultado es positivo, suele continuarse durante varias semanas hasta que la placenta asume su función hormonal.
Si el resultado es negativo, se suspende y se produce la menstruación en los días siguientes.
En los casos en los que inicialmente estaba prevista una transferencia en fresco pero, por motivos clínicos, se decide finalmente vitrificar todos los embriones, la pauta hormonal puede modificarse o suspenderse según el criterio médico. El tratamiento siempre se ajusta a la estrategia final del ciclo.
Entender esta fase ayuda a no interpretar la medicación como un trámite automático. Forma parte activa de la preparación del entorno donde el embrión intentará implantarse.
La transferencia embrionaria: técnica, planificación y coordinación
La transferencia embrionaria es un procedimiento sencillo desde el punto de vista técnico, aunque emocionalmente suele vivirse con intensidad.
Lo ideal es que se realice en un área específica anexa al laboratorio de embriología. Estas salas suelen tener acceso restringido y comunicación directa con el área interna donde se encuentran los incubadores, para minimizar el tiempo de exposición del embrión al exterior.
En muchos centros están protegidas por sistemas de ventilación controlada, filtros de aire y presión positiva, que reducen la entrada de partículas y mantienen condiciones ambientales estables.
La paciente se coloca en posición ginecológica y, bajo control ecográfico abdominal, el médico introduce un catéter muy fino a través del cuello uterino hasta la cavidad uterina. El embrión, suspendido en una pequeña cantidad de medio de cultivo, se deposita cuidadosamente en el interior del útero.
El control ecográfico permite visualizar el trayecto del catéter y orientar el punto de depósito del embrión dentro de la cavidad uterina. Una vez finalizado, el catéter se revisa inmediatamente en el laboratorio para comprobar que el embrión no ha quedado retenido.
Desde las fases previas del tratamiento ya se dispone de información sobre la anatomía uterina y cervical de la paciente.
Durante las ecografías iniciales y, en muchos casos, el mismo día de la punción, el equipo médico valora la orientación del útero (anteverso o retroverso), la longitud del cuello uterino y la facilidad de acceso a la cavidad. Esta información permite anticipar cómo será el trayecto del catéter y elegir el material más adecuado.
La transferencia se realiza bajo control ecográfico abdominal en tiempo real. Por eso se solicita a la paciente que acuda con la vejiga moderadamente llena. La distensión vesical ayuda a rectificar el eje entre el cuello uterino y el cuerpo del útero, facilitando un trayecto más recto del catéter y mejorando la visualización ecográfica.
Si la espera se prolonga o la sensación resulta incómoda, pueden realizarse maniobras para aliviar parcialmente la vejiga sin comprometer la visualización.
En ocasiones el trayecto puede requerir maniobras suaves adicionales. Esto no implica un mal pronóstico. La experiencia del médico y la coordinación con el laboratorio son determinantes para completar el procedimiento con seguridad.
La betaespera: qué ocurre realmente y cómo afrontarla
Tras la transferencia comienza lo que comúnmente se conoce como betaespera: el periodo hasta la realización del análisis de sangre que confirmará si se ha producido la implantación.
Desde el punto de vista biológico, durante estos días el embrión debe completar un proceso complejo. Si se trata de un blastocisto, en las primeras 24–48 horas comienza a interactuar con el endometrio.
La implantación no es un instante, sino una secuencia de eventos que puede extenderse varios días. Solo cuando ese proceso progresa adecuadamente comienza la producción detectable de hormona hCG.
Por eso, realizar pruebas antes de la fecha indicada puede generar resultados confusos. Los niveles hormonales pueden ser todavía demasiado bajos para ser detectados o verse alterados por la medicación utilizada durante el ciclo.
Durante este periodo es frecuente interpretar cualquier sensación corporal como una señal. Molestias abdominales, tensión mamaria, pequeños manchados o ausencia total de síntomas pueden generar interpretaciones anticipadas. Sin embargo, ninguno de estos signos permite confirmar ni descartar un embarazo en esta fase.
Las recomendaciones médicas suelen ser claras: mantener la medicación indicada, evitar esfuerzos físicos intensos durante los primeros días y continuar con una vida cotidiana razonablemente normal. No se recomienda reposo absoluto prolongado, salvo indicación específica.
La betaespera no es un tiempo “vacío”. Es un tiempo en el que el cuerpo está haciendo su parte. Intentar vivirlo con serenidad no significa ignorar la incertidumbre, sino no dejar que la ansiedad la domine.
Preguntas frecuentes sobre la fecundación in vitro
¿La estimulación ovárica afecta a la reserva ovárica a largo plazo?
No. La estimulación no “gasta” óvulos adicionales fuera de lo que ese ciclo ya tenía programado. En cada ciclo natural, varios folículos inician su crecimiento, pero solo uno ovula y el resto se pierde. La FIV rescata parte de esos folículos que de otro modo se reabsorberían. No acelera el envejecimiento ovárico.
¿Existe un número “ideal” de ovocitos para tener buenas probabilidades?
No hay un número perfecto universal. En general, obtener un número suficiente de ovocitos aumenta las probabilidades acumuladas de éxito, pero la calidad es más importante que la cantidad. La edad sigue siendo el factor que más influye en la competencia genética del ovocito.
¿La FIV aumenta el riesgo de malformaciones?
Los estudios científicos disponibles indican que el riesgo global de malformaciones en niños nacidos tras FIV es ligeramente superior al de la población general, pero la diferencia es pequeña y en gran parte se relaciona con las características de las parejas que necesitan tratamiento, no con la técnica en sí. La gran mayoría de los embarazos logrados mediante FIV evolucionan con normalidad.
¿Puede repetirse una FIV inmediatamente si no hay embarazo?
Depende de cada caso. Si existen embriones vitrificados, puede programarse una transferencia en el siguiente ciclo. Si es necesario repetir la estimulación completa, suele recomendarse un intervalo breve para permitir la recuperación ovárica y revisar la estrategia. La decisión se individualiza.
¿El estrés puede hacer que una FIV no funcione?
El estrés no bloquea directamente la implantación ni anula el efecto biológico del tratamiento. Sin embargo, vivir el proceso con ansiedad intensa puede hacerlo más difícil emocionalmente.
Por eso se recomienda acompañamiento, apoyo y estrategias de regulación emocional cuando sea necesario.
¿Cuándo se confirma definitivamente que el embarazo evoluciona bien?
La primera confirmación es la beta-hCG en sangre. Posteriormente, una ecografía alrededor de la semana 6–7 permite visualizar el saco gestacional y la actividad cardíaca embrionaria. Hasta ese momento, la información es progresiva.
Autor
Francisco Carrera
Persona | Experto en Comunicación y Divulgación de la Ciencia (UAM) | Embriólogo Clínico certificado (ASEBIR) | Máster en Biología de la Reproducción Humana (IVIC) | Licenciado en Bioanálisis (UCV).
