Estimulación ovárica en FIV: medicación, duración y seguridad

Una fase decisiva del tratamiento
¿Qué ocurre en el cuerpo durante estos días? ¿Qué medicación se administra? ¿Cómo se sabe si está funcionando? Saberlo no solo aporta seguridad. También ayuda a atravesar el proceso con una mirada más tranquila y confiada.
Qué es la estimulación ovárica?
El objetivo es obtener más ovocitos maduros, y con ellos, más embriones viables que aumenten las probabilidades de lograr un embarazo.
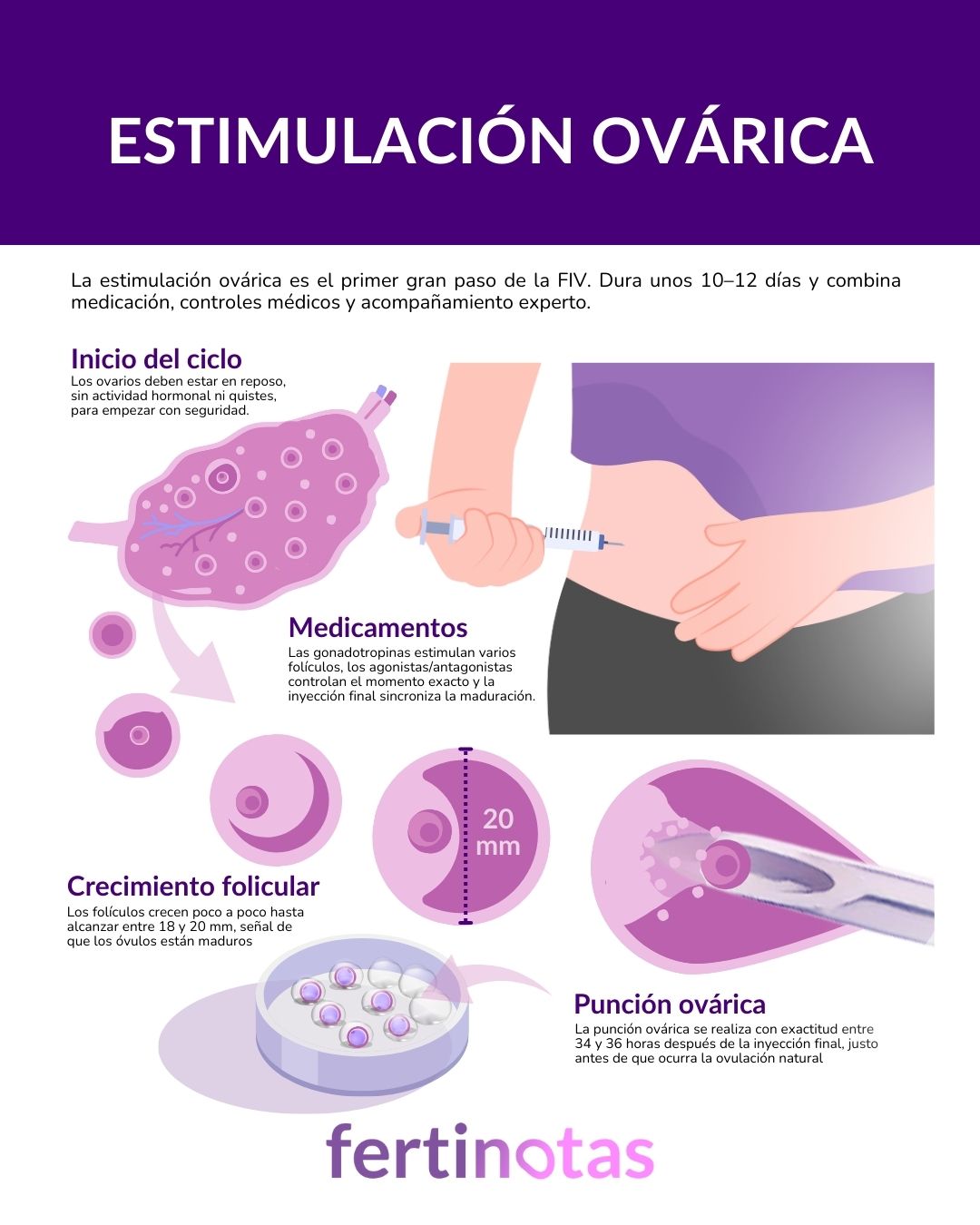
Este proceso dura, por lo general, entre 10 y 12 días. Durante ese tiempo, el equipo médico ajusta la medicación en función de cómo responde cada mujer, valorando ecografías y analíticas para alcanzar el equilibrio ideal entre eficacia y seguridad.
Y aunque la idea de «estimular más» pueda parecer arriesgada, lo cierto es que está respaldada por la ciencia. Un estudio publicado en 2018 demostró que cuantos más ovocitos se recuperan en un ciclo, mayores son las tasas acumuladas de nacidos vivos, especialmente cuando se pueden vitrificar embriones para transferencias posteriores.
Este enfoque no solo mejora la eficacia del tratamiento, sino que también permite planificar el futuro reproductivo con mayor tranquilidad.
¿Qué medicación se utiliza durante la estimulación ovárica?
Aunque el esquema puede variar según cada caso, hay tres tipos fundamentales de fármacos implicados:
• Gonadotropinas: el motor de la estimulación
Son hormonas que estimulan directamente los ovarios para que desarrollen varios folículos a la vez. En condiciones normales, solo uno de ellos suele alcanzar la madurez. Con las gonadotropinas, en cambio, se busca que maduren varios óvulos en un mismo ciclo.
Existen diferentes tipos de gonadotropinas: unas derivadas de la orina humana purificada y otras obtenidas mediante tecnología recombinante. Ambas contienen hormona FSH (hormona foliculoestimulante), y algunas también combinan FSH y LH (hormona luteinizante), cuya presencia puede ser útil en ciertos perfiles.
El tipo, la dosis y la duración del tratamiento con gonadotropinas se ajustan de forma personalizada, teniendo en cuenta la edad, la reserva ovárica y la respuesta en ciclos anteriores.
• Agonistas y antagonistas de GnRH: guardianes del momento justo
Durante la estimulación, existe un riesgo: que el cuerpo desencadene una ovulación espontánea antes de que el equipo médico lo haya planificado. Para evitarlo, se administran medicamentos que controlan la liberación de las propias hormonas del eje hipófiso-ovárico.
Aquí entran en juego los agonistas o antagonistas de GnRH (hormona liberadora de gonadotropinas):
Los agonistas actúan primero estimulando, pero después bloquean la secreción natural de FSH y LH, generando un entorno hormonal más controlado. Se usan sobre todo en protocolos largos.
Los antagonistas, en cambio, bloquean directamente la liberación de LH, lo que permite un control más inmediato y flexible. Son los más empleados en protocolos cortos, por su comodidad y menor riesgo de hiperestimulación.
• Inyección final: el momento clave
Cuando los folículos han alcanzado el tamaño adecuado (entre 18 y 20 mm), se administra una última inyección para inducir la maduración final de los ovocitos. Este paso es crucial, permite que los óvulos completen su desarrollo y estén listos para ser recuperados.
Esta “inyección final” suele contener hCG (gonadotropina coriónica humana) o un agonista de GnRH, y su eficacia depende en gran parte de su sincronización exacta con la siguiente fase, la punción ovárica. Esta intervención se programa unas 34 a 36 horas después de la inyección, justo antes de que se produzca la ovulación natural. Si se hace demasiado pronto o demasiado tarde, los ovocitos podrían perderse o no estar en condiciones óptimas para su fecundación.
Seguimiento y controles durante la estimulación ovárica
¿Qué se vigila exactamente?
El control se basa en dos pilares principales:
• Ecografías transvaginales: permiten observar cuántos folículos están creciendo en cada ovario y medir su tamaño. En una respuesta considerada normal, se espera que los folículos dominantes aumenten su diámetro entre 1,5 y 2 mm por día.
El objetivo es que entre 8 y 15 folículos alcancen un tamaño cercano a los 18–20 mm, lo que indica que contienen ovocitos maduros y listos para ser extraídos.
• Análisis hormonales en sangre: se evalúan principalmente los niveles de estradiol (E2), que reflejan la actividad de los folículos en crecimiento. Como referencia orientativa, se considera una producción de aproximadamente 150–200 pg/mL de estradiol por cada folículo maduro, aunque este valor puede variar según el perfil hormonal de la paciente.
También se mide la progesterona, especialmente hacia el final de la estimulación, ya que un aumento precoz podría alterar el entorno endometrial y comprometer la calidad de la implantación.
En algunos casos, se controlan también los niveles de LH (hormona luteinizante) para descartar picos espontáneos que podrían desencadenar una ovulación prematura, especialmente si no se utilizan antagonistas de GnRH.
¿Por qué es tan importante este seguimiento?
Todo ello permite adaptar el tratamiento a las condiciones reales del cuerpo en tiempo real, maximizando las posibilidades de obtener ovocitos de buena calidad y asegurando que el proceso se desarrolle con la mayor seguridad y eficacia posibles.
¿Qué se siente durante la estimulación?
Más allá de lo físico, la dimensión emocional cobra un protagonismo especial. La ilusión de estar dando un paso decisivo convive con la incertidumbre de los resultados y con el cansancio que pueden generar las visitas médicas frecuentes.
Aun así, muchas mujeres sienten también un tipo particular de entusiasmo: el de observar cómo se desarrollan los folículos, cómo el cuerpo responde, cómo la ciencia multiplica las oportunidades que antes no existían.
Es una vivencia exigente, sí, pero también profundamente transformadora. Y saber que se cuenta con un equipo cercano y comprensivo, con la posibilidad de apoyo psicológico cuando se necesita, ayuda a recorrer este camino con más serenidad, esperanza y gratitud.
Riesgos reales y seguridad actual
Afortunadamente, su incidencia ha disminuido drásticamente en los últimos años gracias al empleo de protocolos modernos, el ajuste individualizado de las dosis hormonales y el uso de agonistas de GnRH como “inyección final”, en lugar de hCG, que reducen el riesgo de respuesta excesiva.
De hecho, una revisión sistemática de Fertility and Sterility (2023) identificó que el uso de antagonistas es una de las intervenciones más efectivas para reducir la incidencia de OHSS, sin comprometer las tasas de embarazo.
Hoy, la prevención del OHSS no solo es posible, sino que forma parte central de la planificación de cada ciclo. Por eso es tan importante que el tratamiento se lleve a cabo en centros con experiencia, donde se combine el rigor clínico con una atención personalizada y atenta a cada detalle.
Un protocolo diseñado para ti
El protocolo corto, basado en antagonistas de GnRH, suele iniciarse al comienzo del ciclo menstrual y es más breve y cómodo. El protocolo largo, en cambio, utiliza agonistas de GnRH e implica más días de preparación, aunque en algunos perfiles puede mejorar la calidad de la respuesta ovárica.
La elección del protocolo no es un detalle menor: influye en la eficacia, en los costes y en la experiencia emocional durante el tratamiento.
Cada cuerpo responde a su manera
Lo esencial es que el equipo médico realice un seguimiento cercano, adaptando el tratamiento en tiempo real y manteniendo expectativas realistas, sin perder de vista que cada óvulo recuperado es una oportunidad.
Avances que mejoran la experiencia
No todas las pacientes son candidatas a utilizarlos, pero en los casos adecuados suponen un gran alivio y mejoran la calidad de vida durante el ciclo.
Cuidados cotidianos y estilo de vida
Antes de iniciar el tratamiento, es habitual que el ginecólogo compruebe que los ovarios están en “reposo”, es decir, sin quistes ni actividad hormonal significativa. Esto asegura que la estimulación arranque en las mejores condiciones posibles.
Costes, tiempos y planificación
Hablar desde el principio sobre precios, tiempos y expectativas ayuda a planificar con más serenidad. Un ciclo de estimulación no es solo una inversión económica, sino también emocional: conocer de antemano qué esperar evita frustraciones innecesarias y facilita un proceso más consciente.
Preguntas frecuentes
¿Cuánto dura la estimulación?
Lo habitual son 10 a 12 días, aunque puede prolongarse o acortarse según la respuesta de cada mujer.
¿Qué diferencia hay entre el protocolo corto y el largo?
El corto comienza al inicio del ciclo menstrual y suele implicar menos días de medicación. El largo se inicia semanas antes, con más preparación hormonal, y puede ser útil en determinados perfiles clínicos.
¿Puedo pedir un tratamiento con menos inyecciones?
En algunos casos sí. Existen fármacos de liberación prolongada que permiten espaciar dosis, aunque deben evaluarse individualmente para comprobar que son seguros y eficaces en tu situación.
¿Qué ocurre si la respuesta ovárica es baja?
Una baja respuesta no significa el final del camino. Se puede ajustar la medicación, probar protocolos distintos, acumular ovocitos en varios ciclos o, llegado el caso, considerar alternativas como la ovodonación.
¿Cómo saber si mi respuesta es “normal”?
Se mide mediante ecografías y análisis hormonales. Lo habitual es que los folículos crezcan entre 1,5 y 2 mm por día y que alcancen alrededor de 18-20 mm antes de la punción. El nivel de estradiol también debe aumentar de forma acorde, reflejando que los óvulos maduran correctamente.
¿Qué cuidados debo tener durante la estimulación?
Además de descansar y mantener hábitos saludables, es clave escuchar al cuerpo. Si aparecen molestias abdominales intensas, dificultad respiratoria o distensión marcada, conviene contactar de inmediato con el equipo médico, ya que podría tratarse de signos de hiperrespuesta ovárica.
Autor
Francisco Carrera
Persona | Experto en Comunicación y Divulgación de la Ciencia (UAM) | Embriólogo Clínico certificado (ASEBIR) | Máster en Biología de la Reproducción Humana (IVIC) | Licenciado en Bioanálisis (UCV).
