PGTA: qué es, para qué sirve y cuándo se recomienda

El procedimiento, conocido como PGT-A, ha sido clave para reducir el riesgo de aneuploidías antes de transferir el embrión al útero. Pero no deja de ser una intervención.
Hoy, una nueva alternativa plantea algo fascinante: ¿y si pudiéramos obtener información genética sin tocar al embrión?
Eso es lo que propone el diagnóstico genético no invasivo preimplantacional de aneuploidías, o niPGTA. Una forma de «escuchar» lo que el embrión deja a su paso.
¿Cómo funciona el niPGTA?
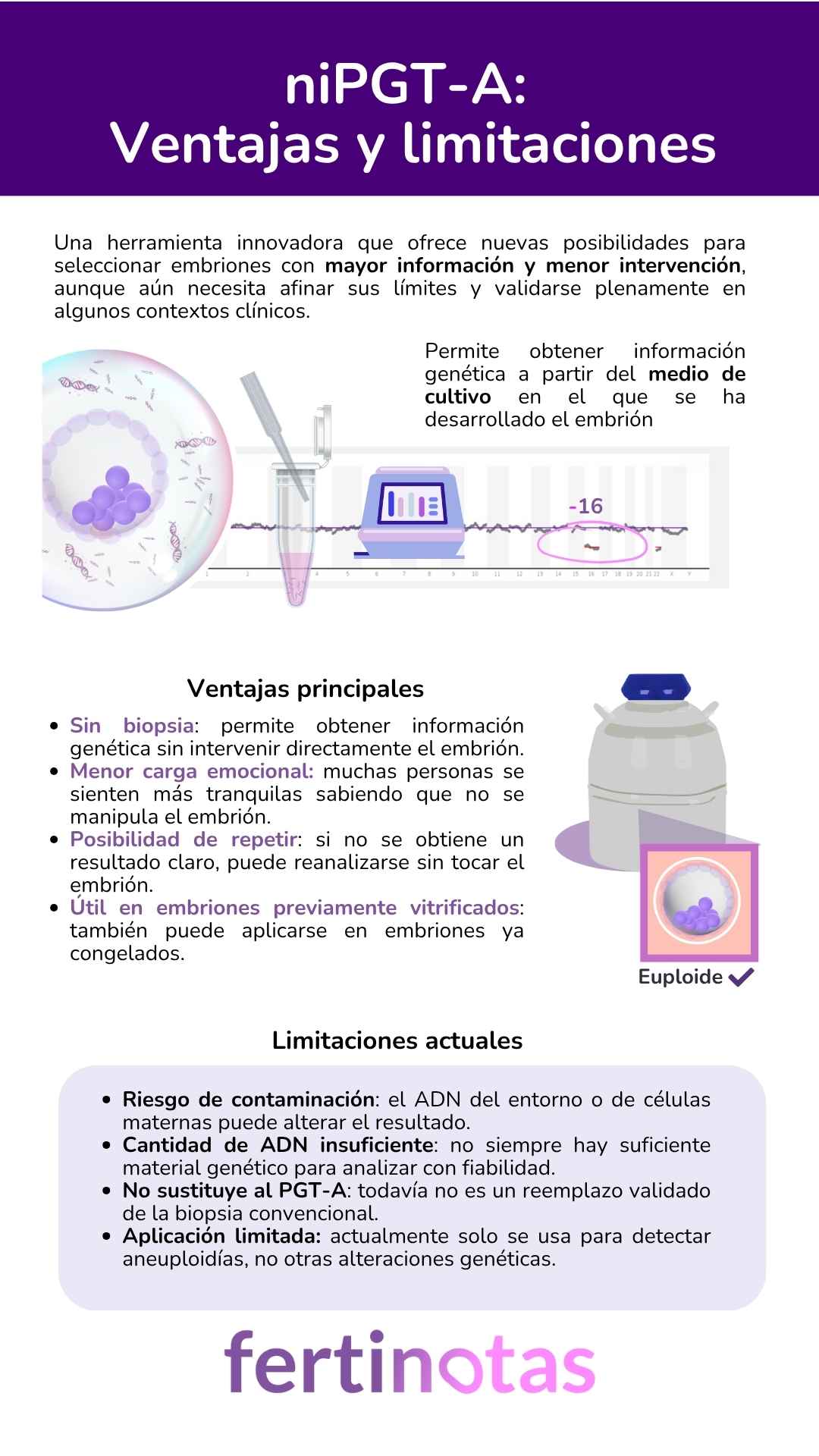
A medida que crecen, van soltando fragmentos diminutos de ADN al líquido que los rodea. Es lo que se conoce como ADN libre de células o cfDNA.
Ese ADN, que podríamos imaginar como migas que el embrión deja en su camino, se recoge al final del cultivo y se analiza mediante técnicas de secuenciación (NGS).
De esta manera, sin tocar al embrión, se puede detectar si tiene una dotación cromosómica normal (euploide) o alterada (aneuploide).
Pero hay algo importante: el resultado no está disponible de inmediato. Mientras se procesa el ADN, los embriones deben ser vitrificados. Es decir, se congelan con una técnica ultrarrápida que conserva toda su viabilidad para transferirlos más adelante.

¿Cómo se interpretan los resultados del niPGTA?
El niPGTA no solo ofrece un resultado binario sobre si un embrión es euploide o aneuploide. Su valor radica, sobre todo, en su utilidad como herramienta de apoyo a la toma de decisiones. Especialmente en ciclos con varios blastocistos vitrificados, puede ayudar a priorizar qué embrión transferir primero.
Esto se debe a que los resultados genéticos obtenidos del medio de cultivo pueden combinarse con otros criterios (como la morfología embrionaria) mediante algoritmos como EMBRACE.
Estos algoritmos generan una puntuación o ranking embrionario que orienta sobre cuál tiene más probabilidad de implantación, sin necesidad de excluir a ningún embrión de entrada.
Ahora bien, interpretar los datos del niPGT-A requiere apoyarse en los estudios de concordancia que han servido como base para validar esta técnica.
Estos estudios comparan los resultados obtenidos del análisis del medio de cultivo (cfDNA) con los del PGT-A tradicional, que se realiza mediante biopsia del trofoectodermo.
Gracias a estas investigaciones, se han podido identificar distintos escenarios posibles:
• Resultados concordantes: tanto el ADN libre del medio como la biopsia indican el mismo diagnóstico (por ejemplo, ambos euploides). En algunos estudios, la concordancia general ha sido alta, especialmente en embriones euploides, con cifras que se ubican entre el 65 y 91 %.
• Resultados discordantes: se detectan diferencias entre el medio y la biopsia, como casos donde el medio indica que el embrión es euploide pero la biopsia detecta una aneuploidía. Estas discordancias son más frecuentes en embriones con mosaicismo o alteraciones complejas, y se consideran uno de los retos actuales del niPGT-A.
• Muestras no informativas: en algunos casos, no se obtiene suficiente cantidad de ADN libre para emitir un resultado fiable. Esto puede depender del tipo de embrión, el tiempo de cultivo o las condiciones del laboratorio.
Estos hallazgos refuerzan la idea de que el niPGTA no sustituye al PGTA convencional, sino que puede actuar como una herramienta complementaria.
Su información orienta y ayuda a priorizar, especialmente en pacientes con embriones vitrificados o que desean evitar la biopsia, pero siempre debe interpretarse dentro del contexto clínico y con asesoramiento profesional.
¿Qué ventajas ofrece el niPGTA?
Aunque aún está en evolución, ya ofrece beneficios concretos que pueden marcar una diferencia en la experiencia reproductiva de muchas personas.
A continuación, exploramos sus principales ventajas, explicadas de forma clara y sencilla.
• Sin biopsia: no requiere extraer células del embrión. Esto significa que no hay intervención directa sobre su estructura, lo cual elimina el riesgo, aunque pequeño, de dañar al embrión durante el proceso.
Además, al no tocarlo, se evita cualquier posible impacto en su desarrollo posterior, lo que tranquiliza a muchas personas que se sienten incómodas con la idea de una manipulación celular.
• Representa mejor al embrión completo: el cfDNA puede reflejar tanto el trofoectodermo como la masa celular interna , es decir, no analiza solo una parte del embrión, sino potencialmente el conjunto.
Esto podría ofrecer una visión más representativa del estado cromosómico global del embrión el cfDNA puede reflejar
• Menor carga emocional: muchas personas prefieren técnicas no invasivas porque les resulta más fácil emocionalmente asumir que el embrión no ha sido manipulado.
Por ejemplo, una pareja que lleva años intentando tener un hijo y que ha tenido que tomar decisiones difíciles en cada paso del tratamiento, puede sentir un gran alivio al saber que, esta vez, no será necesario hacerle nada al embrión.
Esa tranquilidad no es menor: reduce la ansiedad, da más confianza en el proceso y les permite enfocarse en lo que realmente importa.
• Reanalizable: si no hay suficiente ADN, se puede repetir sin tocar al embrión.
• Accesible: no necesita equipamiento de sofisticado para la recuperación del medio de cultivo.
• Válido para embriones vitrificados: esta técnica puede utilizarse incluso en embriones que ya fueron congelados previamente.
¿Cómo?
Una vez que se desvitrifican, se cultivan de nuevo durante unas horas en medio fresco. Ese medio recoge el ADN libre que el embrión sigue liberando tras la descongelación, y puede analizarse como si se tratara de un cultivo convencional.
Esto abre la puerta a reevaluar embriones que, por ejemplo, no fueron analizados en su momento o que dieron resultados no concluyentes.
Es una forma de obtener información genética sin necesidad de biopsiar ni repetir procedimientos invasivos
Limitaciones del niPGTA
Entenderlas es clave para saber cuándo y cómo utilizar esta herramienta de forma segura y realista. Aquí te explicamos las principales:
• Contaminación externa: el medio de cultivo en el que se desarrolla el embrión puede contaminarse con ADN procedente de otras fuentes, como células del cúmulo que rodeaban al óvulo, o incluso del entorno del laboratorio.
Si esto ocurre, el resultado genético podría no reflejar fielmente al embrión. Por eso es fundamental que el laboratorio tenga protocolos estrictos de lavado y manejo para evitarlo.
• Poca cantidad de ADN: a veces no se recoge suficiente cfDNA para obtener un resultado fiable.
• No sustituye al PGT-A: aunque los resultados son prometedores, el niPGT-A todavía no cuenta con suficiente respaldo científico para sustituir por completo al diagnóstico tradicional con biopsia.
Las principales sociedades científicas lo consideran una herramienta complementaria, útil en ciertos contextos clínicos, pero no equivalente.
Como toda técnica emergente, requiere más estudios a gran escala, con seguimiento a largo plazo, antes de integrarse como estándar de rutina
• Aplicaciones limitadas: por ahora, solo se usa para detectar aneuploidías. Su uso para enfermedades monogénicas o reordenamientos cromosómicos está en investigación
¿Qué dicen los resultados clínicos del niPGTA?
Un estudio retrospectivo con más de 270 pacientes con antecedentes de fallos de implantación y pérdidas gestacionales recurrentes mostró que los embriones seleccionados por niPGT-A ofrecieron tasas significativamente más altas de embarazo clínico y en curso que los seleccionados solo por morfología
En otro trabajo más reciente, Sun et al. (2024) compararon tres grupos: selección por morfología, por PGT-A convencional y por niPGT-A. En mujeres entre 35 y 40 años, tanto el PGT-A tradicional como el niPGT-A aumentaron la tasa acumulada de nacidos vivos en comparación con la selección morfológica.
Además, un estudio comparativo de Ocali et al. evaluó más de 2.500 blastocistos analizados por PGT-A convencional y niPGT-A, observando tasas muy similares de euploidía (57.5 % vs. 57.9 %), nacidos vivos (61.0 % vs. 65.7 %) y pérdidas gestacionales (6.2 % vs. 4.3 %), confirmando que el niPGT-A puede ofrecer resultados comparables en muchos contextos clínicos.
Estos datos consolidan al niPGT-A como una herramienta útil en contextos específicos: selección embrionaria más precisa, mejor priorización para transferencia, y en especial, cuando no es viable una biopsia.
niPGTA: una herramienta que se abre camino
Aquí van algunas ideas para orientarte:
Pregunta sin miedo: asegúrate de entender qué información ofrece esta prueba, qué fiabilidad tiene y cómo se va a utilizar en tu caso concreto.
No estás molestando: estás cuidando tu proceso.
Ten en cuenta que no es definitiva: el niPGTA no reemplaza al PGTA tradicional ni garantiza resultados. Aporta datos útiles, pero no siempre concluyentes. Si te dicen que el embrión es euploide o aneuploide, es importante saber con qué grado de certeza se afirma.
Valora si encaja contigo: puede tener mucho sentido si no deseas que manipulen tus embriones, si ya tienes blastocistos vitrificados que no se analizaron o si quieres una herramienta adicional para priorizar.
Confía en el equipo que te acompaña: el verdadero valor del niPGTA está en cómo se interpreta y se aplica a tu situación. Un equipo que te escuche y te explique, marcará la diferencia.
En resumen: el niPGT-A puede ser un aliado. No lo es todo, pero puede ayudarte a dar un paso más con mayor tranquilidad. Tu historia, tus valores y tus deseos deben estar siempre en el centro.
El niPGT-A no es una técnica futurista, ya se aplica en clínicas de todo el mundo.
Aporta información valiosa sin intervenir al embrión y podría convertirse en una opción ideal para muchos casos como pacientes que no pueden o no desean una biopsia, embriones con resultados no concluyentes o ciclos con múltiples blastocistos a priorizar.
Todavía necesita más evidencia y ajustes, pero el camino está abierto.
Y todo apunta a que este tipo de diagnóstico no invasivo formará parte esencial del futuro de la medicina reproductiva.
Autor
Francisco A. Carrera S.
Persona | Experto en Comunicación y Divulgación de la Ciencia (UAM) | Embriólogo Clínico certificado (ASEBIR) | Máster en Biología de la Reproducción Humana (IVIC) | Licenciado en Bioanálisis (UCV).
